11533 – ALANINA AMINOTRANSFERASA (ALT/GPT)
07/20/2022
11539 – COLESTEROL
07/20/202211534 – a-AMILASA (SPECT.CONT)
11534 – a-AMILASA (SPECT.CONT) 1X40 ml

Contáctanos y conoce nuestras áreas de ENVÍO GRATIS en los estados de Jalisco, Guanajuato, Nayarit, Sinaloa y Zacatecas.
Descargar inserto: 11534-α-AMILASA-EPS IFCC 1X40ml
Descarga el catálogo de reactivos de Química Clínica:
11534 – a-AMILASA (SPECT.CONT) 1X40 ml
α-AMILASA-EPS IFCC
Descargar inserto: 11534-α-AMILASA-EPS IFCC 1X40ml
Descarga el catálogo de reactivos de Química Clínica:
FUNDAMENTO DEL MÉTODO
La α-amilasa cataliza la hidrólisis del 4-nitrofenil-maltoheptaósido-etilideno a oligosacáridos,
que son sustratos para la α-glucosidasa, capaz de liberar 4-nitrofenol. La concentración catalítica se determina a partir de la velocidad de formación del 4-nitrofenol, medido a 405 nm1,2.
CONTENIDO
| COD 11582 | COD 11534 | |
|---|---|---|
| A. Reactivo | 1 x 20 mL | 1 x 32 mL |
| B. Reactivo | 1 x 5 mL | 1 x 8 mL |
COMPOSICIÓN
- Reactivo. HEPES 50 mmol/L, cloruro de calcio 0,075 mmol/L, cloruro de sodio 90 mmol/L, cloruro de magnesio 13 mmol/L, α-glucosidasa > 4 U/mL, pH 7,1.
- Reactivo. HEPES 50 mmol/L, 4-nitrofenil-maltoheptaósido-etilideno 18 mmol/L, pH 7,1.
CONSERVACIÓN
Conservar a 2-8oC.
Los reactivos son estables hasta la fecha de caducidad indicada en la etiqueta, siempre que se conserven bien cerrados y se evite la contaminación durante su uso.
Indicaciones de deterioro:
− Reactivos: Presencia de partículas, turbidez, absorbancia del blanco superior a 0,300 a 405 nm (cubeta de 1 cm).
PREPARACIÓN DE LOS REACTIVOS
Reactivo de trabajo: Vaciar el contenido del frasco B en el frasco A. Agitar suavemente. Si se desea preparar otros volúmenes, mezclar en la proporción: 4 mL de Reactivo A + 1 mL de Reactivo B. Estable 20 días a 2-8oC.
MUESTRAS
Suero, plasma u orina recogidos mediante procedimientos estándar.
La α-amilasa en suero o plasma es estable durante 1 mes a 2-8oC. Debe utilizarse la heparina o EDTA como anticoagulante.
La α-amilasa en orina es estable durante 1 mes a 2-8oC siempre que el pH se ajuste aproximadamente a 7 para la conservación.
PROCEDIMIENTO
1. Precalentar el Reactivo de Trabajo y el instrumento a la temperatura de reacción.
2. Pipetear en una cubeta (Notas 1, 2):
| Suero/Plasma | Orina | |||
|---|---|---|---|---|
| 37oC | 30oC | 37oC | 30oC | |
| Reactivo de Trabajo | 1,0 mL | 1,0 mL | 1,0 mL | 1,0 mL |
| Muestra | 30 μL | 60 μL | 15 μL | 30 μL |
3. Mezclar e insertar la cubeta en el fotómetro. Poner el cronómetro en marcha.
4. Al cabo de 1 minuto, anotar la absorbancia inicial y efectuar nuevas lecturas cada minuto durante 3 minutos.
5. Calcular el incremento de absorbancia por minuto promedio (∆A/min).
CÁLCULOS
La concentración de α-amilasa en la muestra se calcula a partir de la siguiente fórmula general:

El coeficiente de absorción molar (ε) del 4-nitrofenol a 405 nm es 10.600 y el paso de luz (l) es 1 cm. Para muestras de suero y plasma, el volumen total de reacción (Vt) es 1,030 a 37oC y 1,060 a 30oC mientras que el volumen de muestra (Vs) es 0,030 a 37oC y 0,060 a 30oC. Para muestras de orina, el volumen total de reacción (Vt) es 1,015 a 37oC y 1,030 a 30oC, y el volumen de muestra (Vs) es 0,015 a 37oC y 0,030 a 30oC. 1 U/L equivale a 0,0166 μkat/L. Se deducen los siguientes factores para calcular la concentración catalítica:

VALORES DE REFERENCIA
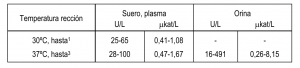
Estos valores se dan únicamente a título orientativo; es recomendable que cada laboratorio establezca sus propios intervalos de referencia.
CONTROL DE CALIDAD
Se recomienda el uso de los Sueros Control Bioquímica niveles I (cod. 18005, 18009 y 18042) y II (cod. 18007, 18010 y 18043), para verificar la funcionalidad del procedimiento de medida.
Cada laboratorio debe establecer su propio programa de Control de Calidad interno, así como procedimientos de corrección en el caso de que los controles no cumplan con las tolerancias aceptables.
CARACTERÍSTICAS METROLÓGICAS
− Límite de detección: 3,0 U/L = 0,05 μkat/L.
− Límite de linealidad: 1300 U/L = 21,6 μkat/L, en suero y 2600 U/L = 43,2 μkat/L en orina.
Cuando se obtengan valores superiores, diluir la muestra 1/5 con agua destilada y repetir la medición.
− Repetibilidad (intraserie):

−Reproducibilidad (interserie):

− Sensibilidad: 0,309 ∆mA⋅L/U⋅min = 18,6 ∆mA ⋅L/μkat⋅min.
− Veracidad: Los resultados obtenidos con estos reactivos no muestran diferencias
sistemáticas significativas al ser comparados con reactivos de referencia. Los detalles del
estudio comparativo están disponibles bajo solicitud.
− Interferencias: La lipemia (triglicéridos 10 g/L) y la bilirrubina (20 mg/dL) no interfieren. La
hemoglobina (10 g/L) interfiere. Otros medicamentos y sustancias pueden interferir4.
Estos datos han sido obtenidos utilizando un analizador. Los resultados pueden variar al
cambiar de instrumento o realizar el procedimiento manualmente.
CARACTERÍSTICAS DIAGNÓSTICAS
La α-amilasa cataliza la hidrólisis de los enlaces α-1,4 de los carbohidratos constituidos por unidades de α-D-glucosa, originando la formación de dextranos, maltosa y glucosa. La α-amilasa se produce principalmente en el pancreas exocrino (tipo-P) y en las glándulas salivales (tipo-S) aunque también se encuentra en otros tejidos.
La medición de la actividad amilasa en suero y orina tiene utilidad principalmente para el diagnóstico de enfermedades pancreáticas como la pancreatitis crónica o aguda. La hiperamilasemia también puede ser debida a insuficiencia renal, dolor abdominal agudo, tumor en pulmones y ovarios, lesiones en las glándulas salivales, macroamilasemia, cetoacidosis diabética, enfermedad del tracto biliar, trauma cerebral, alcoholismo crónico y medicamentos (opiáceos)5,6.
El diagnóstico clínico no debe realizarse teniendo en cuenta el resultado de un único ensayo, sino que debe integrar los datos clínicos y de laboratorio.
NOTAS
1. La saliva y la piel contienen α-amilasa. No pipetear el reactivo con la boca y evitar el contacto del reactivo con la piel.
2. Este reactivo puede utilizarse en la mayoría de analizadores automáticos. Solicite
información a su distribuidor.
BIBLIOGRAFÍA
- Lorentz K. Approved recommendation on IFCC methods for the measurement of calytic concentration of enzymes part 9. IFCC method for α-amylase (1,4-α-D-glucan 4- glucanohydrolase, EC 3.2.1.1). Clin Chem Lab Med 1998;36:185-203.
- Lorentz K. Routine α-amylase assay using protected 4-nitrophenyl-1,4-α-D-maltoheptaoside and a novel α-glucosidase. Clin Chem 2000;46:644-649.
- Junge W, Werner W, Wilke B et al. Development and evaluation of assays for the determination of total and pancreatic amylase at 37 oC according to the principle recommended by the IFCC. Clin Biochem 2001;34:607-615.
- Young DS. Effects of drugs on clinical laboratory tests, 4th ed. AACC Press, 1995.
- Tietz Textbook of Clinical Chemistry, 2nd edition. Burtis CA, Ashwood ER. WB Saunders
Co., 1994.
- Friedman and Young. Effects of disease on clinical laboratory tests, 3th ed. AACC Press, 1997.
Descargar inserto: 11534-α-AMILASA-EPS IFCC 1X40ml